臨床研究は、その目的や実施方法によって、従うべき規制が異なります。実施しようとする臨床研究がどの規制に該当するかは以下のチャートを参考に各規制を確認した上で判断してください。
判断が困難な場合は、未来医療開発部統一相談窓口か各委員会事務局にご相談ください。
このような臨床研究に関するお困りの方は、研究相談窓口にご連絡ください。
以下によくあるご質問とその回答を掲載しています。
事前に確認の上、右側の「研究相談窓口はこちら」のバナーより相談をお申込みください。
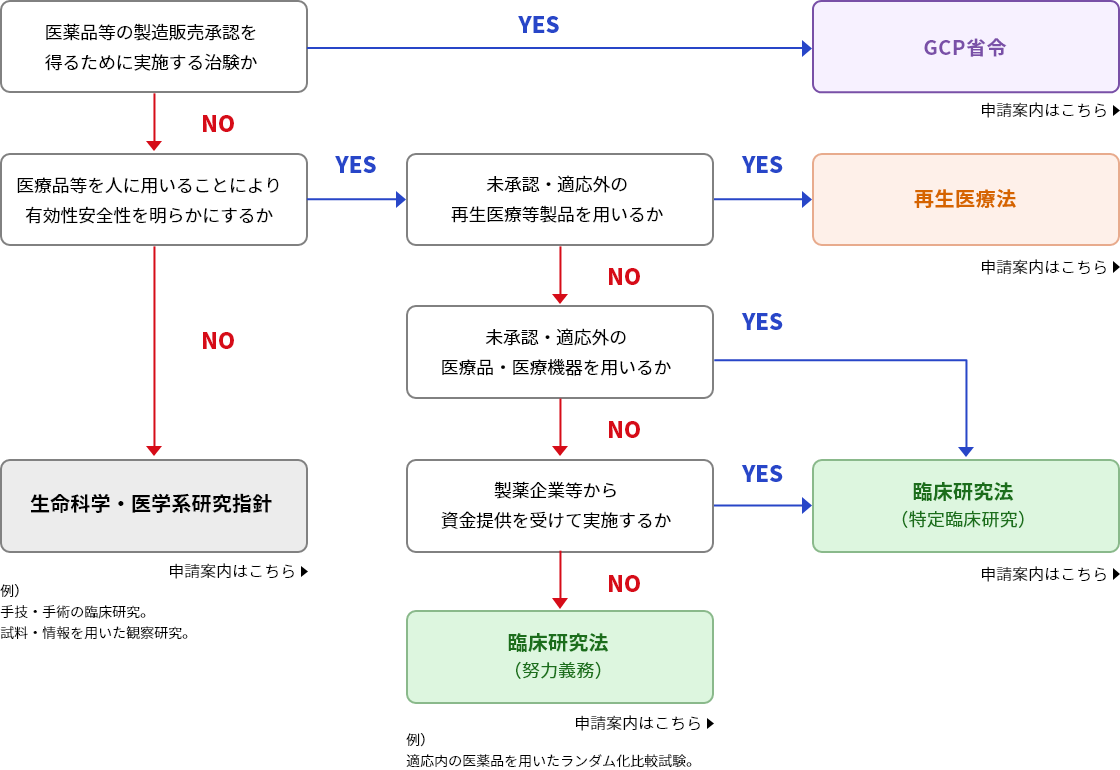
臨床研究は、その目的や実施方法によって、従うべき規制が異なります。実施しようとする臨床研究がどの規制に該当するかは以下のチャートを参考に各規制を確認した上で判断してください。
判断が困難な場合は、未来医療開発部統一相談窓口か各委員会事務局にご相談ください。

すでに学術的な価値が高まり、研究用として広く利用され、一般的に入手可能な細胞を用いる研究は審査不要です。
(例 HeLa細胞、ヒト由来細胞から樹立したiPS細胞のうち研究材料として提供されているもの)
なお、提供機関から倫理審査が求められる場合は、倫理審査委員会にご申請ください。
すでに学術的な価値が高まり、研究用として広く利用され、一般的に入手可能なデータを用いる研究は審査不要です。
(例 米国疾病対策センター(CDC)のダウンロード可能な研究用データベースの情報、査読された学術論文に掲載されている情報、著者が公開している原資料で研究用に広く利用可能となっている情報)
健康や疾病等の理解、予防方法、診断方法、治療方法を検証することで、医学的に新たな知識を得るために行う活動であれば、「生命科学・医学系研究」に該当しますので、倫理審査委員会にご申請ください。
特定の個人と対応関係が排斥されている統計情報など、個人の情報に該当しない場合は、審査不要です。
医療の一環(研究目的でない)とみなすことができる場合は、生命科学・医学系研究に該当しないため、審査不要です。
他の医療従事者への情報共有を図るため、所属する機関内の症例検討会、機関外の医療従事者同士の勉強会や関係学会、医療従事者向け専門誌等での個別の症例を報告する場合も同様です。
なお、学会等から倫理審査が求められる場合は、倫理審査委員会にご申請ください。
精度管理が自施設における医療の質の確保であれば、研究目的でない医療の一環とみなすことができ、生命科学・医学系研究に該当しないため、審査不要ですが、測定機器の開発等、研究目的であれば審査が必要です。個々の事例について検討する必要がありますので、研究相談窓口までお問い合わせください。
ライブ手術などの臨床倫理に関する審査は医学系研究科・医学部医学倫理委員会で行っております。
詳細は下記までお問い合わせください。
(問い合わせ先)
医学系研究科総務課企画係
i-soumu-kikaku(at)office.osaka-u.ac.jp
※(at)は@に置き換えてください。
細胞を人に投与する場合のみ、再生医療法の対象となりますので、動物への投与は対象外です。
しかし、新たに人から採取した細胞を用いてiPS細胞を作製する場合は、生命科学・医学系研究となりますので、倫理審査委員会にご申請ください。
用いるiPS細胞が研究材料として提供されているものである場合は、Q2をご確認ください。
なお、動物実験を行う場合は、別途申請が必要ですので、下記までお問い合わせください。
(動物実験に関する問い合わせ先)
医学系研究科総務課企画係
i-soumu-kikaku(at)office.osaka-u.ac.jp
※(at)は@に置き換えてください。
医師主導治験は、製薬企業のように医師自ら治験を企画・立案し、治験計画届を提出して治験を実施します。医師主導治験では医師自らが、治験実施計画書等の作成から始まり、治験計画届の提出、治験の実施、モニタリングや監査の管理、試験結果を取りまとめた総括報告書の作成など、実施医療機関と協力しながら治験のすべての業務の実施並びに統括しなければなりません。
実施を検討されている場合、研究相談窓口までお問い合わせください。
認定臨床研究審査委員会(CRB)にて審査後、jRCTに登録の上、病院長の実施許可を受ける必要があります。別途利益相反確認の手続きも必要です。
特定臨床研究は、多施設共同研究の場合でも、一つのCRBにて一括審査となります。
●当院が単施設あるいは代表施設の場合
原則、当院のCRBにご申請ください。特段の理由があり、当院以外のCRBに諮る必要がある場合は、審査前に病院長の許可が必要ですので、教育研究支援課までご連絡ください。
(連絡先)
教育研究支援課
rin-sokatu(at)dmi.med.ossaka-u.ac.jp
※(at)は@に置き換えてください。
●当院が分担施設の場合
代表施設が選定したCRBの審査を受けた後、病院長の実施許可を受けてください。
詳細はこちらをご参照ください。
なお、阪大では委員会前にブラッシュアップ会議にて研究計画・申請形態などの事前チェックを⾏っております。当院の研究者のみならず、当院以外の研究者からの相談にも対応しておりますので、実施を検討されている場合、研究相談窓口までお問い合わせください。
倫理審査委員会にて審査後、病院長の実施許可を受ける必要があります。
別途利益相反審査の手続きも必要です。
委員会審査、病院長への実施許可の申請は、自主臨床電子申請システムより行ってください。
詳細は
こちらをご参照ください。
当院では先進医療や患者申出制度などの「保険外併用療養費制度」(保険診療と保険外診療との併用を認め、将来的な保険導入に向けた評価を行う制度)を利用した研究開発または臨床研究を支援しております。
保険収載等に向けた研究開発または臨床研究をご計画の際には研究相談窓口までお問い合わせください。
原則、E-learningシステムであるCROCOにて該当するコースを受講してください。
コースは、実施する臨床研究の種類に応じて、
臨床研究法、生命科学・医学系研究指針、治験、再生医療等がございます。
2年目以降はポイント制となっておりますので、必要なポイントを取得してください。
詳細は、
こちらをご確認ください。
規制に応じてご用意しております。
臨床研究法(学内専用)
・プロトコル
・同意説明文書
・総括報告書
・研究対象者識別コードリスト
生命科学・医学系指針
・プロトコル、説明文書、同意書、同意撤回書、オプトアウト文書
企業治験
・同意説明文書
医師主導治験
・同意説明文書
再生医療法
・総括報告書
臨床研究利益相反審査委員会に申告が必要です。
規制や審査を行う委員会によって、申告様式、提出先が異なります。
手続きは
こちら(学内専用)よりご確認ください。
研究者自身が保険代理店に連絡し、補償賠償保険にご加入ください。
国大協サービスを用いる場合は、保険の見積もり等は教育研究支援課を通して行ってください。
健康被害の発生による補償申し立てがあった場合は、直ちに教育研究支援課へご相談ください。
(連絡先)
教育研究支援課研究支援係
ibyou-sien-sien(at)office.osaka-u.ac.jp
※(at)は@に置き換えてください。
国内未承認薬、研究費等で購入あるいは製薬会社等から提供された医薬品については薬剤部にて管理します。
詳細は
こちらをご参照ください。
契約の種類によって異なります。なお、治験の契約は治験の申し込みと合わせた手続きとなります。
●臨床研究法の契約
医学部附属病院教育研究支援課総括係へご連絡ください。
契約書式をご用意しております。事前にこちらをご確認ください。
●共同研究、受託研究契約
医学部附属病院の場合は教育研究支援課総括係、医学系研究科の場合は経理課外部資金第二係へご連絡ください。
共同研究のお手続きはこちらをご確認ください。
受託研究のお手続きはこちらをご確認ください。
(医病 担当部署連絡先)
教育研究支援課総括係
電話番号 06-6210-8277
メールアドレス ibyou-sien-soukatu(at)office.osaka-u.ac.jp
※(at)は@に置き換えてください。
(医学系研究科 担当部署連絡先)
経理課外部資金第二係
電話番号 06-6879-3027
メールアドレス i-keiri-gaibu2(at)office.osaka-u.ac.jp
※(at)は@に置き換えてください。
企業治験の場合は、治験事務局にて手続きを行います。
臨床研究、医師主導治験の場合は、診療科にて、大阪大学謝金規則に則り、謝金システムにてお手続きください。
詳細は
謝金マニュアル等をご確認ください。
臨床研究については、該当する診療科へご相談ください。
治験については、治験事務局にメールでお申し込みください。
手続きの詳細は
こちらをご確認ください。
支援の一例です。
・プロトコル等の書類作成
・登録・割付、データマネジメント、統計解析業務
・EDC構築
・臨床研究コーディネーターによる同意取得補助やEDC入力等の業務サポート
・モニタリングまたは監査業務
・研究事務局業務
・上記支援のコーディネート など
臨床研究の種類や予算によって、最適な支援内容をご提案します。
支援に必要な費用は、準拠する規制、研究デザイン、施設数、症例数、研究期間、支援の内容によって異なります。
概算となりますが、支援料のシミュレーションをご利用ください。
ただし、支援内容、支援料ともにあくまで目安としてお考えください。
見積りの相談も承っておりますので、ご希望の場合は研究相談窓口までお問い合わせください。
未来医療試験ユニット(Clinical Trial Unit)をご利用いただけます。
未来医療試験ユニットは阪大病院内にあり、10床のベッドルーム、洗面室・シャワールーム、食事や娯楽等くつろぎスペースであるホール、診察室、ナースステーション、機材・検査室を完備しております。
ご希望の方は、研究相談窓口までお問い合わせください。
事前に秘密保持契約を締結することは可能です。
契約書の様式は任意です。実際に支援、相談を行う部署の担当者にご依頼ください。
生命科学・医学系指針下で行われる研究に関して、原則、研究計画書の事前確認は行っておりません。直接、倫理審査委員会にご申請ください。
臨床研究法に該当する場合、利益相反委員会・臨床研究審査委員会の申請前にブラッシュアップ会議にて試験計画・申請形態などの事前チェックを行います。
臨床研究法下で行われる臨床研究を計画される場合、研究相談窓口までお問い合わせください。
当部データセンターにてCDCSを利用した研究に関する相談を承っております。ご希望の場合は、研究相談窓口にお問合せください。
REDCapは、研究者が簡単にWeb上でデータベースの構築と管理ができ、多施設のデータを簡単かつ安全に収集できるシステムです。
詳細は
REDCapポータルサイトをご確認ください。
当部データセンターで承っております。
臨床研究または基礎研究における統計解析に関することでお悩みの方は研究相談窓口までお問い合わせください。
当部ではOCRネットを利用した研究に関する支援も行っております。
ご希望の場合、研究相談窓口にお問合せください。
未来医療開発部未来医療センターでは、基礎研究、応用研究、非臨床試験、臨床試験等の開発段階に応じて、各種研究開発相談、特許申請支援、PMDA相談等の支援、細胞製品製造支援等を行っています。これら支援を得るには橋渡しシーズとしての登録が必要です。まずは研究相談窓口までお問い合わせください。
未来医療開発部未来医療センターでは、実用化に向けた研究開発に関する初期的な相談を受け付けています。まずは研究相談窓口までお問い合わせください。(この段階では橋渡しシーズとしての登録は不要です)
未来医療開発部は文部科学省認定橋渡し研究支援機関として、橋渡し研究実施のための研究費(AMED異分野融合シーズ・シーズA・シーズB・シーズC等)の研究費支援や獲得支援を実施しています。
研究費獲得のためのシーズ公募は
こちらをご確認ください。
未来医療開発部未来医療センターでは、RS総合相談、RS戦略相談等のPMDA相談の支援を実施しています。
ご希望の場合、研究相談窓口までお問い合わせください。
未来医療開発部未来医療センターでは、シーズの医師主導治験等で必要な治験薬概要書やプロトコールの作成の支援・相談を実施しています。
ご希望の場合、研究相談窓口までお問い合わせください。
未来医療開発部未来医療センターでは、医療機器開発に関して研究開発の戦略、薬事・保険戦略等の相談や支援、企業に対する医療現場ニーズ探索の支援等を実施しています。
ご希望の場合、研究相談窓口までお問い合わせください。
未来医療開発部未来医療センターでは、細胞治療、遺伝子治療等の再生医療等製品の実用化を積極的に支援しています。細胞調製施設は、学外のアカデミアや企業も利用可能となっています。ご希望の場合、研究相談窓口までお問い合わせください。
大阪大学における特許出願の手続きの詳細は共創機構ホームページをご確認ください。
未来医療開発部未来医療センターでは、特許出願や知財戦略立案を含む、実用化に向けた研究開発に関する相談を受け付けており、共創機構医学系分室の担当者とも連携しています。ご希望の場合、研究相談窓口にお問合せください。
大阪大学におけるベンチャー創成支援制度は共創機構ホームページをご確認ください。
未来医療開発部未来医療センターでは、大学発ベンチャーと連携して医療技術として実用化を目指す研究開発を積極的に支援しています。ご希望の場合、研究相談窓口にお問合せください。
開発初期の事業化戦略の策定、臨床研究、治験、再生医療等を進める上で発生する諸課題(薬事・保険適用を含む)に関して、企業だけで検討するのが困難な事例等に関して、当部の担当者複数名との面談(直接 or WEB)により、課題の解決の検討を行うことができます。(1回の時間は最大2時間まで)
相談の内容により、対応する担当者は決定して対応しますが、内容によっては、お答えが難しく、ご対応いたしかねるものもあるかと思いますので、あらかじめ、ご了承の程よろしくお願いします。
初回時の相談は基本的には無償(1回30分程度)です。
(内容によっては、初回から有償で対応させていただくこともあります。)
ご希望の方は、研究相談窓口までお問い合わせください。
まずは、研究室の主宰者、共同研究者等と研究データの取り扱いについて協議してください。共同研究契約や外部資金等に基づく研究については契約内容を確認してください。論文化の際の著者の所属についても投稿先のルールも参考に検討してください。
以下は研究の規制上必要な対応です。
●研究実施中の場合
異動先を研究機関に追加し、データを共有してください。
●研究終了後の場合
データがすでに統計解析されており統計データのみであれば倫理審査等の対応は不要です。症例報告書(データ化されたものも含む)や解析用データセットであり、異動後に解析を行う場合は研究活動となりますので、異動先の機関で倫理審査等を受けた上で行ってください。
なお、論文化された後の研究データについては、大阪大学における研究データの保存等に関するガイドライン及び各部局の関連するガイドラインの規定に従いデータ保存が必要となります。
また、研究データを持ち出す場合は、仮名加工、匿名加工等の適切な加工を行い、個人情報に配慮することが必要です。